

市值观察SZGC
研发日上,维立志博创始人康小强的一句话让人印象深刻:任何一个千亿级的Biotech都不是一上市就是千亿的公司,它一定是经过了几年的发展,我相信维立志博未来可期。$维立志博-B(HK|09887)$
说实话,我看完整个研发日才真正理解这句话的含金量。当看到公司计划在2026年下半年至2027年同时推进4个大三期临床时,才明白“几年的发展”意味着什么。
先说重点,4个三期临床具体是:
. LBL-024一线肺外神经内分泌癌(EP-NEC)
. LBL-024一线非小细胞肺癌(NSCLC)
. LBL-024一线胆道癌(BTC)
. LBL-034复发/难治性多发性骨髓瘤(RRMM)
三期临床不是想开就能开的
从临床开发到上市,一款新药平均耗时10-15年、耗资超过20亿美元,而最终成功商业化的概率不足12%。三期临床是整个链条中最贵的环节,单适应症投入可达数千万至上亿美元。这种背景下,企业敢开三期临床,必须同时满足几个硬条件:
一是前期数据必须足够强。II期或概念验证研究的数据必须呈现出明确、一致的疗效趋势,且安全性可控。这不是“有点效果”就能拍的板。
二是监管路径必须清晰。需要与监管机构反复沟通,确认注册路径可行。三期临床一旦启动,相当于锁定了证据包,调整空间极小。
三是差异化优势必须明确。相比现有标准治疗,必须有显著的治疗获益预期,否则即使做出来也没有市场竞争力。
所以,启动三期不是喊口号,而是数据驱动下的确定性投资。
拆解4个三期临床:数据说话
LBL-024(PD-L1/4-1BB):四个维度验证基石疗法,三期临床水到渠成
EP-NEC是典型冷肿瘤,CSCO指南及NCCN指南在二线以后就没有任何系统治疗方案推荐了。维立志博计划在这个适应症推进III期确证性临床,底气在哪里?
为什么一口气开三个适应症的三期?因为LBL-024作为IO 2.0泛肿瘤基石疗法的核心能力,已经在安全性、泛肿瘤有效、冷肿瘤攻坚、拖尾效应四个维度上被充分验证,而EP-NEC、NSCLC、BTC三个适应症的拓展也非常符合维立志博“末线推向一线、罕见病推向大瘤种”的递进逻辑。
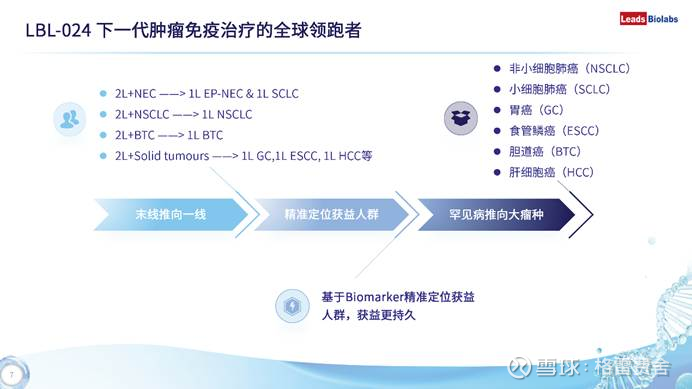
先看四个维度的数据底子:
. 安全性:超600例患者,整体安全性与PD-1单抗相当,攀升至25mg/kg仍无剂量限制性毒性。这是三期大样本、长周期用药的前提。
. 泛肿瘤有效:正在开展覆盖13个实体瘤适应症的1项关键注册临床研究和8项POC研究,已在EP-NEC、NSCLC、SCLC、BTC中展示出FIC/BIC潜力。这说明已经有显著且稳健的疗效信号支持三期临床的开展。
. 冷肿瘤有效:EP-NEC和BTC都是典型冷肿瘤,LBL-024单药在末线EP-NEC上已推进至BLA阶段,疗效自不必说。
. 拖尾效应:末线EP-NEC中位OS翻倍至11.9个月,一线EP-NEC也观察到OS延长趋势,有望让肿瘤患者真正实现长期生存获益。
再看三个适应症各自的前期数据和差异化优势:
. EP-NEC:从无药可用到突破性数据
二线及以上无标准疗法,LBL-024末线单药ORR 33.3%、mOS 11.9个月(现有疗法的2倍);一线联合化疗ORR 83.3%(II期剂量优化阶段15mg/kg组)。数据足够颠覆,且已获CDE突破性疗法认定、FDA孤儿药认定和快速通道资格、欧盟孤儿药认定,三期是顺势而为。
. NSCLC:从罕见病推向大瘤种
全球最大实体瘤市场,PD-L1低表达及阴性患者占60%以上,现有PD-1效果有限。LBL-024一线NSCLC的临床研究由张力牵头。研发日公布了此前18例可评估受试者随访延续数据,总体ORR高达72.2%。其中,免疫经治非鳞癌患者ORR仍达75%,直观展示出LBL-024和IO1.0基石药PD-(L)1抑制剂之间存在着根本性的疗效代差。一线非鳞癌和一线鳞癌的ORR分别为83.3%和62.5%,相比年报公布的数据有进一步提升,表明随着时间延长,缩瘤效应一直在持续,有望获得深度且持久的缓解。一旦三期成功,估值锚点将从罕见病切换到大癌种,乘数效应不言而喻。
. BTC:冷肿瘤的又一验证
BTC恶性程度高、进展快、预后极差,5年生存率低于5%。PD-1/L1抑制剂联合化疗虽是晚期胆道恶性肿瘤的一线治疗方案,但总生存期的获益有限(中位生存期从大约11.5个月提升到12.8个月),客观缓解率(ORR)仍不足30%。LBL-024胆道癌的临床研究由复旦大学附属中山医院周俭院士牵头,在这一适应症上已完成安全性导入期20例受试者完成初步评估,并于近期顺利进入扩展阶段。
把这三个适应症放在一起看:EP-NEC是“敲门砖”+“冷肿瘤模板”,NSCLC是“最大增量市场”,BTC是“复制冷肿瘤成功经验”。 三期临床同时推进,不是烧钱博概率,而是数据驱动的确定性决策——安全性经得起放大,疗效信号在多个瘤种中交叉验证,差异化机制(PD-L1/4-1BB双靶点)相比现有PD-1单抗有本质优势。
今年9月WCLC将公布大样本一线NSCLC数据,10月ESMO将公布末线EP-NEC单臂关键注册临床研究数据、联合化疗一线治疗EP-NEC的进一步数据、一线BTC数据,届时市场将迎来重要验证节点。
LBL-034(GPRC5D/CD3):比肩CAR‑T,但无需“私人定制”
CAR-T疗法在RRMM中的疗效毋庸置疑,但单次治疗费用超40万美元,国产CAR-T疗法约100-129万人民币/次,且需要数周“私人定制”周期。
LBL-034在400-1200μg/kg剂量组12个月PFS率达61.2%,微小残留病(MRD)阴性率80%,伴髓外病变ORR 75%,既往BCMA靶向治疗失败患者ORR 85.7%。疗效堪比CAR-T,更重要的是安全性更高,且秒杀同类竞品。剂量递增至1200μg/kg剂量级,未观察到DLT,未达到最大耐受剂量(MTD),多数治疗期间不良事件(TEAE)发生在第1周期且有自愈倾向,不影响治疗的连续性,不对患者的生活质量造成不利影响。
无需个体化制备,成本和患者便利性更优,不影响生活质量,患者依从性更高,LBL-034一旦获批上市,对现有疗法的冲击力可想而知。
对投资人意味着什么?
4个三期临床同时推进,传递的信号很清楚:
. 确定性跃升。一家Biotech同时启动4个大三期临床,不是烧钱任性,而是前期疗效信号足够强、研发平台足够稳健的必然选择。投资决策的底层逻辑从“能不能有效”切换到“能不能获批,市场有多大”。风险等级明显降维。
. 催化剂密集度提升。4个三期临床意味着未来2-3年将有多个关键数据读出节点,WCLC、ESMO年会、BLA申报……每一个都是可追踪的价值验证节点。
. 估值框架再评估。 从“单一罕见病管线”到“多适应症III期临床+平台协同”,市场很可能因此对维立志博的估值逻辑做出相应调整。
2026年下半年至2027年,维立志博将进入“商业兑现+临床纵深”双轮驱动的全新发展阶段。按创始人在研发日上的说法,维立志博已经走过了10年,下一个10年是发展更快的10年。4个三期大临床的密集启动,或许正是这个全新篇章的起点。
本文基于研发日公开信息及公司披露材料整理,不构成投资建议。
用户在证星号发表的信息将由本网站记录保存,仅代表作者个人观点,与本网站立场无关,不构成投资建议,据此操作风险自担
